Reactiesnelheid
Een chemische reactie is het gevolg van een botsing tussen deeltjes. Doordat deze botsingen plaatsvinden kunnen bindingen breken en kunnen nieuwe verbindingen gevormd worden. Hierdoor kan dan een herschikking van de atomen gebeuren.
Een effectieve botsing gebeurt wanneer de deeltjes voldoende energie alsook een juiste oriëntatie hebben zodat er een reactie kan gebeuren.
De activeringsenergie Ea is de energie die men moet toevoegen om de reactie te starten.
De factoren die de reactiesnelheid beïnvloeden:
– Concentratie: hoe hoger de concentratie van deeltjes, hoe meer effectieve botsingen er kunnen zijn en hoe sneller de reactie kan verlopen. Snelheidsvergelijking: v=k⋅[A]⋅[B]. k stelt hierin de reactieconstante voor. Voor elke reactie moet men de snelheidsvergelijking experimenteel vaststellen.
– Druk: als bij gassen de druk toeneemt zal ook de concentratie toenemen waardoor we terug bij het voorgaande geval terechtkomen.
– Temperatuur: als de temperatuur stijgt, gaan de deeltjes sneller bewegen (kinetische energie neemt toe). Doordat deze snelheid toeneemt zullen er meer effectieve botsingen plaatsvinden.
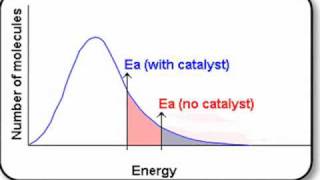
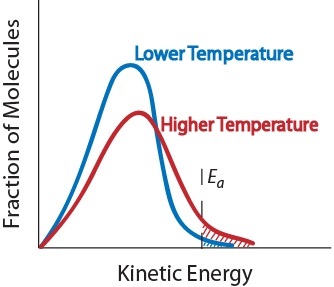
Op nevenstaande grafiek is duidelijk gemaakt dat de fractie moleculen met energie voldoende om te reageren afhankelijk is van de temperatuur.
– Contactoppervlakte/verdelingsgraad: Als de reagentia fijner verdeeld worden is het contactoppervlak tussen de reagentia vergroot. De verhouding tussen het oppervlak en het volume neemt toe naarmate de stof fijner verdeeld is
Een groter contactoppervlak betekent meer botsingen tussen de deeltjes en dus een hogere reactiesnelheid.
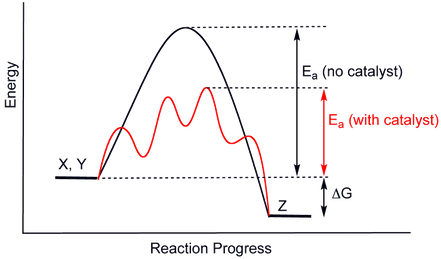
– Katalysator: een katalysator heeft een invloed op de reactiesnelheid maar neemt zelf niet deel aan de reactie. D.m.v. een katalysator wordt een andere reactieweg gevolgd tijdens de reactie. Deze alternatieve weg is gekenmerkt door een kleiner activeringsenergie dan in een niet gekatalyseerde reactie. Doordat Ea kleiner is hebben ook meer deeltjes van de reagentia voldoende kinetische energie om aanleiding te geven tot een effectieve botsing.
Een effectieve botsing gebeurt wanneer de deeltjes voldoende energie alsook een juiste oriëntatie hebben zodat er een reactie kan gebeuren.
De activeringsenergie Ea is de energie die men moet toevoegen om de reactie te starten.
De factoren die de reactiesnelheid beïnvloeden:
– Concentratie: hoe hoger de concentratie van deeltjes, hoe meer effectieve botsingen er kunnen zijn en hoe sneller de reactie kan verlopen. Snelheidsvergelijking: v=k⋅[A]⋅[B]. k stelt hierin de reactieconstante voor. Voor elke reactie moet men de snelheidsvergelijking experimenteel vaststellen.
– Druk: als bij gassen de druk toeneemt zal ook de concentratie toenemen waardoor we terug bij het voorgaande geval terechtkomen.
– Temperatuur: als de temperatuur stijgt, gaan de deeltjes sneller bewegen (kinetische energie neemt toe). Doordat deze snelheid toeneemt zullen er meer effectieve botsingen plaatsvinden.
Op nevenstaande grafiek is duidelijk gemaakt dat de fractie moleculen met energie voldoende om te reageren afhankelijk is van de temperatuur.
– Contactoppervlakte/verdelingsgraad: Als de reagentia fijner verdeeld worden is het contactoppervlak tussen de reagentia vergroot. De verhouding tussen het oppervlak en het volume neemt toe naarmate de stof fijner verdeeld is
Een groter contactoppervlak betekent meer botsingen tussen de deeltjes en dus een hogere reactiesnelheid.
– Katalysator: een katalysator heeft een invloed op de reactiesnelheid maar neemt zelf niet deel aan de reactie. D.m.v. een katalysator wordt een andere reactieweg gevolgd tijdens de reactie. Deze alternatieve weg is gekenmerkt door een kleiner activeringsenergie dan in een niet gekatalyseerde reactie. Doordat Ea kleiner is hebben ook meer deeltjes van de reagentia voldoende kinetische energie om aanleiding te geven tot een effectieve botsing.
Enzymen zijn eiwitten die in biochemische reacties optreden als biokatalysatoren.
Het feit dat enzymen eiwitten zijn, betekent dat zij net zo gevoelig zijn voor milieufactoren als alle andere eiwitten. Als eiwitten te heet worden, verliezen ze hun structuur; dat noem je denatureren. Bij het denatureren verandert de vorm van het eiwit. Dit is een onomkeerbare gebeurtenis: het eiwit gaat kapot. Je kunt dat heel goed zien als je een ei kookt. Door de hitte wordt het doorschijnende eiwit ondoorschijnend wit en hard.
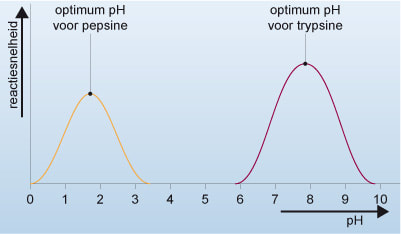
Een gedenatureerd enzym is niet meer in staat een substraat op de juiste manier te binden. De reactie kan dan ook niet meer plaatsvinden. Een eiwit denatureert niet alleen bij extreem hoge temperaturen, maar ook bij een zuurgraad (pH) als die sterk afwijkt van de normale werkomstandigheden van het eiwit.
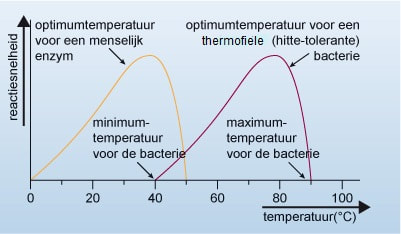
Het gevolg van deze eigenschappen is dat enzymen alleen kunnen werken als de waarden van de temperatuur en de pH tussen bepaalde grenzen liggen. De ondergrens wordt het minimum genoemd. We onderscheiden dus een minimumtemperatuur en een minimum-pH. De bovengrens is het maximum. Tussen minimum en maximum ligt het optimum (= de beste waarde).
Bij een optimale temperatuur en bij een optimale pH werkt het enzym het beste. Onder optimumomstandigheden wordt dus per tijdseenheid de grootste hoeveelheid substraat omgezet.
Het feit dat enzymen eiwitten zijn, betekent dat zij net zo gevoelig zijn voor milieufactoren als alle andere eiwitten. Als eiwitten te heet worden, verliezen ze hun structuur; dat noem je denatureren. Bij het denatureren verandert de vorm van het eiwit. Dit is een onomkeerbare gebeurtenis: het eiwit gaat kapot. Je kunt dat heel goed zien als je een ei kookt. Door de hitte wordt het doorschijnende eiwit ondoorschijnend wit en hard.
Een gedenatureerd enzym is niet meer in staat een substraat op de juiste manier te binden. De reactie kan dan ook niet meer plaatsvinden. Een eiwit denatureert niet alleen bij extreem hoge temperaturen, maar ook bij een zuurgraad (pH) als die sterk afwijkt van de normale werkomstandigheden van het eiwit.
Het gevolg van deze eigenschappen is dat enzymen alleen kunnen werken als de waarden van de temperatuur en de pH tussen bepaalde grenzen liggen. De ondergrens wordt het minimum genoemd. We onderscheiden dus een minimumtemperatuur en een minimum-pH. De bovengrens is het maximum. Tussen minimum en maximum ligt het optimum (= de beste waarde).
Bij een optimale temperatuur en bij een optimale pH werkt het enzym het beste. Onder optimumomstandigheden wordt dus per tijdseenheid de grootste hoeveelheid substraat omgezet.
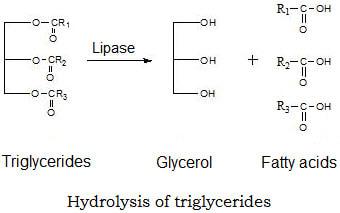
het enzym lipase
Pancreatine is een mengsel van enzymen dat wordt geproduceerd in de alvleesklier. Het bevat amylase, lipase en protease. Amylase dient voor de afbraak van zetmeelmoleculen, protease voor de afbraak van eiwitten en lipase voor de afbraak van vetten.
Het lipase enzym kan vetmoleculen of triglyceriden splitsen in een glycerolmolecule en 3 vetzuren. Ze verbreken de esterverbindingen in triglyceriden door middel van hydrolyse (= reactie met water).
Vetten kunnen niet zomaar oplossen in het water, maar enzymen kunnen dit weer wel. Om lipase dus te laten inwerken op vetten moet het vet in hele kleine druppels verdeeld worden. Dit kan alleen door hulp van een emulgator, zoals bijvoorbeeld ossengal dat in staat is om vetbolletjes te verdelen in kleinere vetbolletjes zodat de oppervlakte waarop lipase kan inwerken vergroot.
Lipase heeft een pH optimum van 8,0.
Lipase heeft een pH optimum van 8,0.