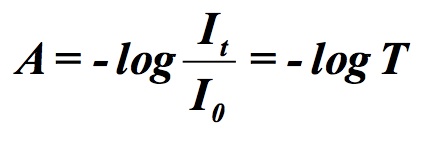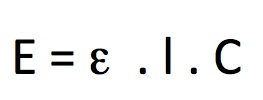Doel van de proef
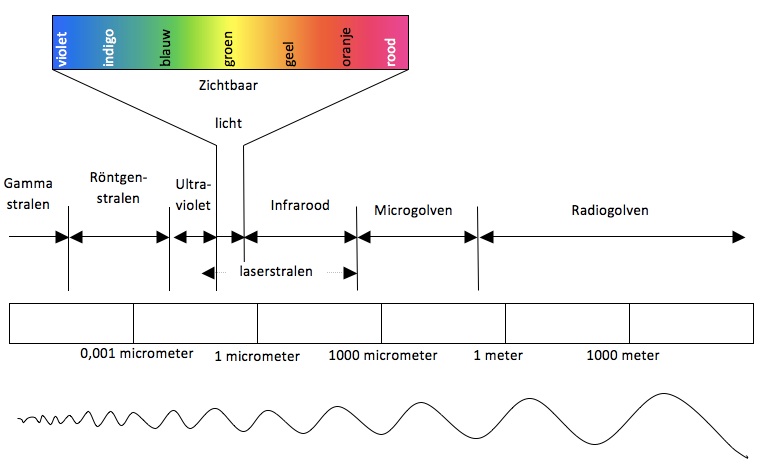
- Licht als deel van het elektromagnetisch spectrum zien.
- Het principe van de spectrofotometer doorhebben.
- Via een staalname van een kleurstaal inschatten waar gaat geabsorbeerd worden.
Inleiding
Hoewel het zichtbare licht slechts een zeer kleine plaats inneemt in het totaal van het elektromagnetische spectrum speelt het toch een zeer belangrijke rol bij waarneming en in analytische meettechnieken.
Kleurstoffen absorberen bepaalde golflengtes van het spectrum. Alleen de niet-geabsorbeerde golflengtes worden teruggekaatst, bereiken onze ogen en geven de sensatie van kleur. De niet geabsorbeerde golflengtes en wel geabsorbeerde golflengtes vormen complementaire kleuren.
We herkennen een oplossing als ‘blauw’ omdat ze vooral golflengten van 435 tot 480 nm doorlaat en de andere absorbeert.
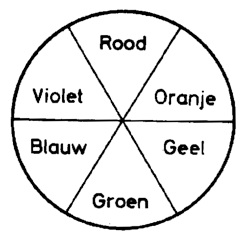
De kleur van een oplossing is dus steeds complementair aan de kleur van de golven die het meest geabsorbeerd worden. Complementaire kleuren zijn per definitie kleuren die met elkaar gemengd wit licht geven.
We herkennen een oplossing als ‘blauw’ omdat ze vooral golflengten van 435 tot 480 nm doorlaat en de andere absorbeert.
De kleur van een oplossing is dus steeds complementair aan de kleur van de golven die het meest geabsorbeerd worden. Complementaire kleuren zijn per definitie kleuren die met elkaar gemengd wit licht geven.
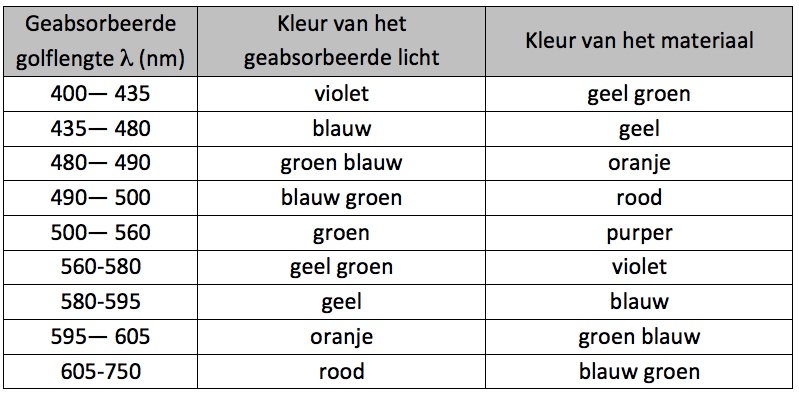
Hieronder vind je een tabel met golflengtes, bijhorende kleuren en complementaire kleuren.
|
Wanneer blauw licht (monochromatisch licht) door een blauwe oplossing gestuurd wordt, dan zal dit praktisch niet afgezwakt worden.
Bij doorzenden van wit licht (polychromatisch licht) door een blauwe oplossing zullen andere golflengten zoals oranje en rood meer opgeslorpt worden. De grootste absorptie gebeurt echter met de gele band uit het spectrum (559-580 nm). We zeggen dat geel de complementaire kleur is van blauw. Omgekeerd is blauw de complementaire kleur van geel. |
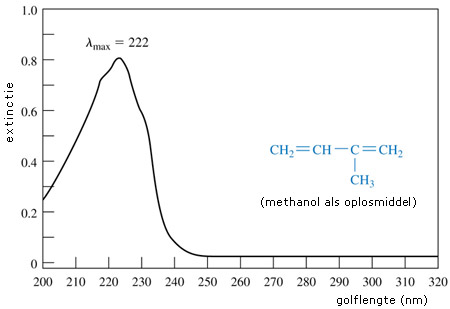
Het absorptiespectrum
Transmissie en absorbantie
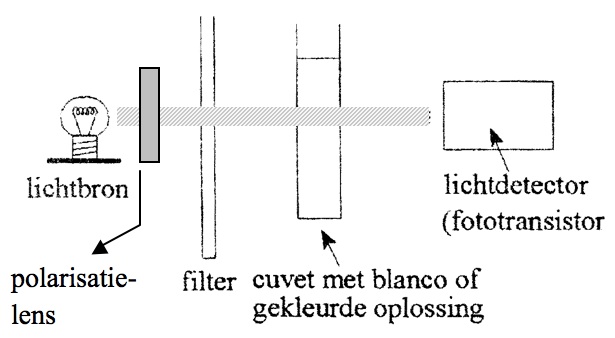
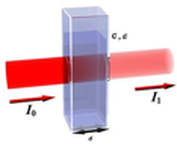
Om toch enig inzicht te krijgen in wat zich afspeelt in de spectrofotometer volgt een heel korte uitleg. Men stuurt een monochromatische (1 frequentie) lichtbundel met een bepaalde intensiteit (I) door een oplossing die een kleurstof bevat.
Via een lichtdetector wordt de lichtintensiteit die door de oplossing gaat gemeten.
Om toch enig inzicht te krijgen in wat zich afspeelt in de spectrofotometer volgt een heel korte uitleg. Men stuurt een monochromatische (1 frequentie) lichtbundel met een bepaalde intensiteit (I) door een oplossing die een kleurstof bevat.
Via een lichtdetector wordt de lichtintensiteit die door de oplossing gaat gemeten.
|
De hoeveelheid al dan niet geabsorbeerd licht wordt uitgedrukt via de grootheden transmissie (T) en absorbantie (A).
De transmissie is een maat voor het doorgelaten licht. Transmissie is de verhouding van de hoeveelheid licht die door de oplossing doorgelaten wordt (It) t.o.v. de hoeveelheid licht die door de blanco doorgelaten wordt (I0) De blanco is het oplosmiddel zonder kleurstof. |
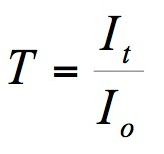
De absorptie is een maat voor het geabsorbeerde licht. De absorbantie is de negatieve logaritme van de transmissie.
De spectrofotometer loopt de verschillende golflengtes af en meet telkens de transmissie voor de blanco (I0) en voor de cuvet met de onbekende stof (It). Voor elk punt wordt dus de absorbantie berekend:
De wet van Lambert-Beer De wet van Lambert-Beer stelt:
l is de dikte van de vloeistof of in dit geval de cuvetdikte.
C is de concentratie (mol/L)
epsilon is de molaire extinctiecoëfficiënt. Wanneer C in mol/l en l in cm is uitgedrukt is de eenheid van e: l.mol.cm-1.
Epsilon is constant voor een bepaalde absorberende stof maar afhankelijk van
- oplosmiddel
- temperatuur
- golflengte van het gebruikte licht
Aangezien voor een bepaalde stof lengte l en e vastliggen, is er dus een verband tussen A en C.
Hiervan kan gebruik gemaakt worden om concentraties in oplossingen te bepalen.